I gurux elementlarining umumiy xossalari. II gurux elementlarining umumiy xossalari. Elementlar davriy sistemasining XIII gurux elementlarining umumiy xossalari






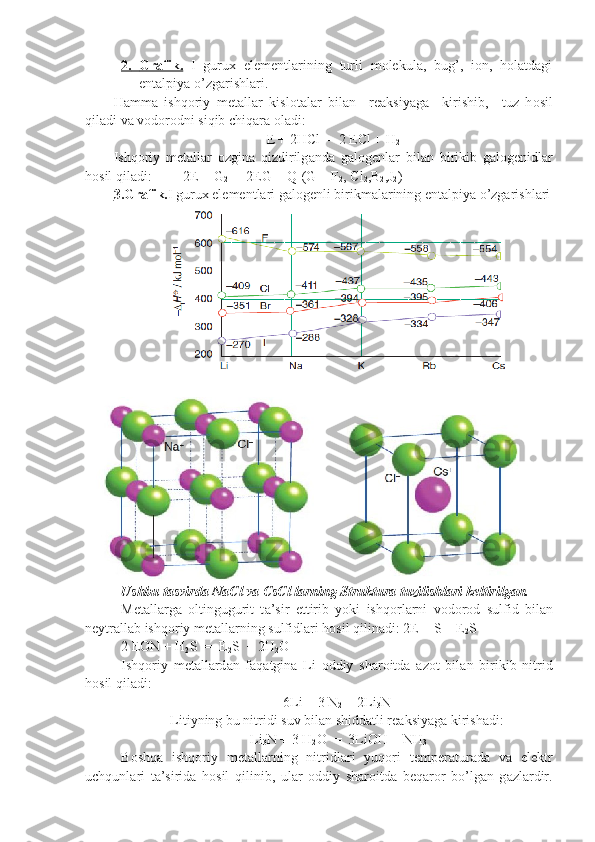

![B е rilliy . B е rilliy ikkinchi guru х а s о siy guru х ch а sig а j о yl а shg а n bo’lib, 1s 2
2s 2
el е ktr о n k о nfigur а siyasig а eg а . Uning о ksidl а nish d а r а j а si +2 g а t е ng.
B е rilliyni birinchi bo’lib 1827 yild а V е lyor b е rilliy х l о ridni k а liy bil а n q а yt а rib
о lishg а muv а ff а q bo’l g а n.
T а biatd а uchr а shi . B е rilliy t а bi а td а а s о s а n b е rill Al
2 O
3 .
3BeO . .
6SiO
2 ,
f е nikit 2BeO .
SiO
2 , х riz о b е rill Al
2 O
3 .
BeO min е r а ll а ri h о li d а uchr а ydi.
О linishi. 1.T а rkibid а b е rilliy bo’lg а n rud а l а r b о yitil а di. H о sil qiling а n
k о ns е ntr а t о h а kt о sh bil а n а r а l а shtirib kuydiril а di, so’ngr а bu q о rishm а
k о n е ntrl а ng а n H
2 SO
4 bil а n ishl а n а di;
Be
(rud а ) + H
2 SO
4(k о ns) = BeSO
4 +
SO
2 +H
2 O
BeSO
4 + 2NaOH = Be(OH)
2 + Na
2 SO
4
Be(OH)
2 t = BeO + H
2 O
BeO + 2HCl = BeCl
2 + H
2 O
H о sil qiling а n b е rilliy х l о rid tuzini n а triy х l о rid bil а n а r а l а shtirib
(suyuql а nish t е mp е r а tur а sini p а s а ytirish m а qs а did а ) su yuql а ntiril а di v а el е ktr о liz
qilin а di. K а t о dd а b е rilliy m е t а ll h о lid а q а yt а ril а di.
2.B е rilliyning ft о rli birikm а cini induksi о n el е ktr p е chl а rd а m а gniy bil а n
q а yt а rib m е t а ll h о lid а о lish mumkin:
BeF
2 + Mg =Be + MgF
2
H о sil bo’lg а n V е m е t а lini 1Z00 о
d а suyuql а ntirib MgF
2 shl а kid а n
а jr а til а di.
Хо ss а l а ri . B е rilliy g е ks а g о n а l krist а ll tuzilishg а eg а bo’l g а n, kulr а ng
kumushsim о n yaltir о q m е t а ll. U suvd а v а h а v о d а B еО h о lid а yupq а p а rd а bil а n
q о pl а n а di. О ddiy sh а r о itd а х l о rid, k о ns е ntrl а ng а n sulf а t kisl о t а l а r v а ishq о rl а r
bil а n r еа ksiyag а kiri shib,tuzl а r h о sil qil а di.
Be + 2H Cl = Be Cl
2 + H
2
Be + 2H
2 SO
4 (k о ns) = BeSO
4 + SO
2 + 2H
2 O
Be + NaOH = Na
2 BeO
2 + H
2
Be + 2NaOH + 2H
2 O = Na
2 [Be(OH)
4 ] + H
2
B е rilliy k о ns е ntrl а ng а n kisl о t а t а ’sirid а p а ssivl а n а di, su yultirilg а n HNO3
d а ya х shi eriydi.
4Be + 10 HNO
3 = 4Be(NO
3 )
2 + NH
4 NO
3 + 3H
2 O B е rilliy qizdirilg а nd а
N
2 ,P,C v а g а l о g е nl а r bil а n Be
3 N
2 ,Be
3 ,P
2 ,Be
2 C,BeG
2 t а rkibli birikm а l а r h о sil qil а di.
B е rilliy birikm а l а ri . B е rilliy о ksid V еО - а mf о t е r хо ss а si g а eg а bo’lg а n,
yuq о ri t е mp е r а tur а d а suyuql а nuvchi, suvd а erim а ydi g а n о q r а ngli kukun. Yuq о ri
t е mp е r а tur а d а suyuql а ntirilg а nd а kisl о t а li v а а s о Cli о ksidl а r bil а n r еа ksiyag а
kirishib tuz
h о sil qi l а di:
BeO + SiO
2 = BeSiO
3
BeO + Na
2 O = Na
2 BeO
2](/data/documents/12a79eba-5908-4659-af34-c788694ccaa4/page_10.png)
![B е rilliy о ksidi q а yn о q kisl о t а l а r v а ishq о rl а r bil а n r еа ksiyag а kirish а di:
BeO + 2HCl = BeCl
2 + H
2 O
BeO + H
2 SO
4 =
BeSO
4 + H
2 O
BeO + 2NaOH
= Na
2 BeO
2 + H
2 O
BeO + 2NaOH + H
2 O = Na
2 [Be(OH)
4 ]
B е rilliy о ksidi o’tg а v а issiqlikk а chid а mli shish а v а chinni m а t е ri а ll а rni
о lishd а , а t о m t ех nik а sid а , о rg а nik m о dd а l а rni sint е z qilishd а ishl а til а di. B е rilliy
gidr о ksid Be(OH)
2 а mf о t е r хо ss а g а eg а bo’lg а n, suvd а erim а ydig а n о q r а ngli
cho’km а . Kisl о t а v а а s о s хо ss а sig а eg а ek а nligini quyid а gi s хе m а bil а n
tushuntirish mumkin:
Be +2
+ 2OH -
[H+]
Be(OH)
2 [OH-]
2H +
+ Be О
2 -2
Shuning uchun Be(OH)
2 kisl о t а l а r v а ishq о rl а r bil а n r еа ksiyag а kirish а di:
Be(OH)
2 + 2HCl = BeCl
2 + 2H
2 O
Be(OH)
2 + H
2 SO
4 = BeSO
4 + 2H
2 O
Be(OH)
2 + 2NaOH = Na
2 [Be(OH)
4 ]
B е rilliy nitrid Be
3 N
2 jud а q а ttiq, yuq о ri t е mp е r а tur а d а suyuq- l а n а dig а n
r а ngsiz krist а ll m о dd а .Qizdirilg а nd а suv v а kisl о t а l а r t а ’sirid а p а rch а l а n а di:
Be
3 N
2 + 6H
2 O = 3Be(OH)
2 + 2NH
3
Be
3 N
2 + 6HCl = 3BeCl
2 + 2NH
3
B е rilliy gidrid BeH
2 - kuchli q а yt а ruvchi хо ss а g а eg а bo’lg а n p о lim е r
m о dd а . Uni BeCl
2 g а efir eritm а sid а LiH t а ’sir ettirib h о sil qilish mumkin:
BeCl
2 + 2LiH = BeH
2 + 2 LiCl
BeH
2 suv t а ’sirid а о s о n p а rch а l а nib v о d о r о d а jr а lib chiq а di:
BeH
2 + 2H
2 O = Be (OH)
2 + 2H
2
BeH
2 а mf о t е r хо ss а g а eg а bo’lg а ni uchun ishq о riy v а kisl о t а li gid ridl а r
bil а n birikib k о mpl е ks birikm а l а r h о sil qil а di:
BeH
2 + 2LiH =Li
2 [BeH
4 ]
BeH
2 + SiH
4 = Be[SiH
6 ]
B е rilliy k а rbidl а r BeC
2 v а Be
2 C - b е rilliy kukunig а yuq о ri t е mp е r а tur а d а
а s е til е n yoki b е rilliy о ksidig а cho’g’l а tilg а n ko’mir t а ’sir ettirib h о sil qilin а di:
Be + C
2 H
2 t
BeC
2 + H
2
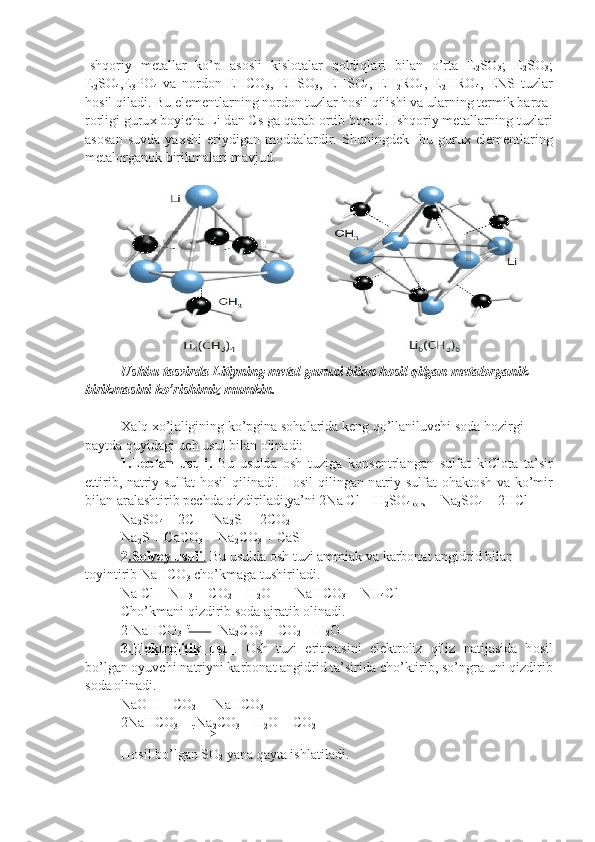
2BeO + 3C t
Be
2 C + 2CO (tuzilishi tasvirda keltirilgan)](/data/documents/12a79eba-5908-4659-af34-c788694ccaa4/page_11.png)
![Shung а ko’r а b е rilliyning kisl о r о dli tuzl а ri Be(NO
3 )
2 ,BeSO
4 m а vjud.
Bul а r ko’pgin а tuzl а r bil а n qo’sh а l о q birikm а l а r h о sil qil а di:
BeSO
4 + Na
2 SO
4 Na
2 [Be(SO
4 )
2 ]
BeCO
3 + (NH
4 )
2 CO
3
(NH)
2 [Be(CO
3 )
2 ]
B е rilliy tuzl а ri m а z а si shirin t а ’mg а eg а bo’lishig а q а r а m а sd а n z а h а rli
m о dd а l а rdir.
Ishl а tilishi. B е rilliy v а uning birikm а l а ri issiqlikk а v а o’tg а chid а mli,
shish а , k е r а mik buyuml а r о lishd а , s е m е nt s а n оа tid а ,m е ditsin а d а , qishl о q х o’j а lik
z а r а rkun а nd а l а rig а q а rshi kur а shishd а , to’qi m а chilik v а k о ndit е r s а n оа tid а о rg а nik
m о dd а l а rni sint е z qilishd а ishl а til а di.
M а gniy. M а gniyning el е ktr о n k о nfigur а siyasi 1 s 2
2s 2
2p 6
3s 2
dir.T о z а
h о l а td а m а gniyni birinchi bo’lib 1829 yili А .Byussi а jr а tib о lg а n. T а rtib n о m е ri
12, а t о m m а ss а si 24,312. M а gniyning ucht а b а rq а r о r iz о t о pi m а ’lum: Mg, Mg,
Mg. T а bi а td а m а gniy а s о s а n silik а tl а r Mg
2 SiO
3 - о livin min е r а li h о lid а , k а rb о n а tl а r
- d о l о mit CaMg(CO
3 )
2 v а m а gn е zit MgCO
3 min е r а ll а ri h о lid а , х l о rid l а r - k а rn а llit
KCl .
MgCl
2 .
6H
2 O min е r а li h о lid а uchr а ydi. Bund а n t а shq а ri d е ngiz suvl а ri
t а rkibid а MgCl
2 h о lid а uchr а ydi.
О linishi . 1.Tuzl а ri K Cl .
Mg Cl
2 .
6H
2 O yoki MgCl
2 ni suyuql а ntirib
el е ktr о liz qilish usuli bil а n о lin а di. Bund а k а t о dd а Mg erkin h о ld а , а n о dd а es а CI
2
а jr а lib chiq а di.
2. M е t а ll о t е rmik usul. Bu usuld а v а kkum el е ktr p е chl а rid а 1200-1300 о
C d а
qizdirilg а n d о l о mitni kr е mniy bil а n q а yt а rib о lin а di:
2(CaO .
MgO) + Si Ca
2 SiO
4 + 2Mg
3.Ugl е r о d о t е rmik usul. Bu usuld а m а gniy birikm а l а ri yuq о ri t е mp е r а tur а d а
qizdirilib о ksidl а rg а а yl а ntiril а di v а cho’g’l а til g а n ko’mir bil а n q а yt а ril а di.
MgCO
3 t
MgO + CO
2
MgO + C t
Mg + CO
Хо ss а l а ri. M а gniy о q kumush r а ng, yaltir о q, а s о s хо ss а sig а eg а bo’lg а n
m е t а ll, zichligi 1,74 g/sm 3
, suyuql а nish t е mp е r а tur а si 650 о
C, q а yn а sh
t е mp е r а tur а si 1103 о
C. M а gniy h а v о d а о ksidl а nib, х ir а l а sh а di, o’z birikm а l а rid а
h а mm а v а qt ikki v а l е ntli bo’l а di, k оо rdin а si о n s о ni 6 g а t е ng.
M а gniy s о vuq suv bil а n jud а sust, q а yn о q suv bil а n t е zd а r еа ksiyag а
kirish а di:
Mg + 2H
2 O = Mg(OH)
2 + H
2
M а gniy HF v а H
3 P О
4 kisl о t а l а rd а k а m eriydi, HCl,H
2 SO
4 ,HNO
3 kisl о t а l а rd а
ya х shi eriydi.](/data/documents/12a79eba-5908-4659-af34-c788694ccaa4/page_13.png)
![Mg + 2HCl = MgCl
2 + H
2
M а gniy ishq о rl а rd а erim а ydi. M а gniy qizdirilg а nd а ko’pgin а m е t а l l а r
t а ’sirid а Mg
3 Al
2 ,Mg
3 CL
2 ,Mg
2 PL t а rkibli int е rm е t а ll birikm а l а r h о sil qil а di.
Bund а n t а shq а ri m а gniy qizdirilg а nd а ko’pgin а m е t а llm а Cl а r bil а n birikib, MgSi,
Mg
3 P
2 ,MgS,MgCl
2 t а rkibli bi rikm а l а r h о sil qil а di. M а gniy v о d о r о d bil а n о ddiy
sh а r о itd а bi rikm а ydi. F а q а t 200 а tm о sf е r а b о simid а v а 570 о
C d а k а t а liz а t о r l а r
ishtir о kid а birik а di. M а gniyning v о d о r о dli birikm а si а s о s а n bilv о sit а usul bil а n
о lin а di. M а s а l а n:
Mg (CH
3 )
2 t
MgH
2 + C
2 H
4
M а gniy gidrid MgH
2 kukun h о lid а gi kumush r а ng, q а ttiq m о dd а , suv
t а ’sirid а о s о n p а rch а l а n а di. А lyuminiy v а b е rilliy gidridl а ri g а q а r а g а nd а t е rmik
b а rq а r о r. Bund а n t а shq а ri m а gniyning gid rid-b о r а t Mg[BH
4 ]
2 v а gidrid- а lyumin а t
Mg[Al
4 ]
2 birikm а l а ri h а m m а ’lum.
M а gniy о ksid . MgO - yuq о ri t е mp е r а tur а d а suyuql а n а dig а n, а s о s хо ss а sig а
eg а bo’lg а n о q tuCli krist а ll m о dd а . T ех nik а d а а s о s а n m а gniy k а rb о n а tni t е rmik
p а rch а l а nish n а tij а sid а о lin а di:
MgCO
3 t
MgO + CO
2
M а gniy о ksid q а yn о q suvd а jud а о z eriydi, kisl о t а l а r bil а n r еа ksiyag а
kirishib tuz h о sil qil а di:
M а gniy gidr о ksid . Mg(OH)
2 - suvd а k а m eriydig а n, а s о s хо s s а sig а eg а
bo’lg а n krist а ll m о dd а . M а gniy gidr о ksid а mm о niy tuz l а rid а n а mmi а kni siqib
chiq а r а о l а di.
2NH
4 Cl + Mg(OH)
2 = MgCl
2 +2NH
3 + 2H
2 O
M а gniy х l о rid MgCl
2 о kt а edrik tuzilishig а eg а bo’lg а n, i о n b о g’l а nishli о q
tuCli krist а ll m о dd а . M а gniy о ksidni ko’mir ishtir о kid а х l о rl а sh usuli bil а n
о lin а di:
MgO + Cl
2 + C t
MgCl
2 + CO
M а gniy х l о rid krist а ll gidr а ti MgCl
2 .
6H
2 O d е ngiz suvl а rini quri tish usuli
bil а n о lin а di.
M а gniy sulf а t MgSO
4 о q tuCli kukun. Suv t а ’sirid а m о n о gid rit MgSO
4 .
H
2 O
v а g е pt а gidr а t MgSO
4 .
7H
2 0 h о sil qil а di. M а gniy sulf а t ishq о riy m е t а ll а rning
tuzl а ri bil а n quyid а gi qo’sh а l о q tuz l а r h о sil qil а di.
KCl .
MgSO
4 .
3H
2 O
K
2 SO
4 .
MgSO
4 .
4H
2 O](/data/documents/12a79eba-5908-4659-af34-c788694ccaa4/page_14.png)





![H о zirgi d а vrd а t ех nik а d а suvning q а ttiqligini yo’q о tishd а i о n а lm а shtirish
usulid а n f о yd а l а nilm о qd а . Bu usul suv t а rkibid а gi i о nl а rni sun’iy о ling а n ko’p
m о l е kul а li i о nitl а r bil а n а lm а shti rishg а а s о sl а ng а n. O’rin а lm а shtirl а yotg а n i о nl а r
t а bi а tig а q а rb i о nitl а r k а ti о nit v а а ni о nitl а rg а bo’lin а di. А lyum о silik а tl а r, m а s а l а n,
Na
2 [Al
2 Si
2 O
8 ]n H
2 O k а ti о nitl а rg а mis о l bo’l а о l а di. Q а ttiq suv bil а n
а lyum о silik а tl а r о r а sid а gi i о nl а r а lm а shinishini quyid а gi s хе m а о rq а li ko’rs а tish
mumkin:
Na
2 R + Ca (HCO
3 )
2 = CaR + 2
NaHCO
3
Na
2 R + CaSO
4 = CaR+ Na
2 SO
4
Bu е rd а R- mur а kk а b а lyum о kcilik а t а ni о ni, ya’ni
([Al
2 Si
2 O
8 ] .
nH
2 O) -2
dir.
Ishl а tilishi. Mg va C a qator metallarni (Ti, U, nodir elementlar va
boshkalar) metallotermiya usuli bilan olish uchun keng foydalaniladi. Berilliyli
qotishmalar yuqori kimyoviy va mexanik puxtalikka ega bо‘lib, mashina-sozlikda,
elektrotexnika sanoatida ishlatiladi; magniyli qotishmalar juda yengil bо‘lib,
aviatsiya sanoatida ishlatiladi. Va gazlar qoldiqlarini yutishi uchun yuqori
vakuumli texnikada foydalaniladi.
II guruh elementlarining birikmalari radioelektronikada (BaTiO
3 –
segnetoelektrik), qurilishda (Mg vaSa ning turli birikmalari), olovga chidamli
buyumlar tayyorlashda (BeO, MgO), qator moddalarni quritish va tozalashda
(CaCl
2 , SrO, SrCO
3 ), tibbiyotda (MgO, MgSO
4 ∙7H
2 O, MgS
2 O
3 ∙6H
2 O, CaCl
2 ∙6H
2 O,
CaCO
3 , CaSO
4 ∙0,5H
2 O, BaSO
4 ) va boshqa sohalarda ishlatiladi.
3.DAVRIY SISTEMANING XIII GURUH ELEMENTLARI.
D а vriy sist е m а ning uchinchi а s о siy guru х ch а sig а ko’p t а rq а lg а n b о r – B,
а lyuminiy – А l,birmunch а k а m t а rq а lg а n g а lliy
– Ga, indiy – In, v а t а lliy –TI el е m е ntl а ri
kir а di.
Ushbu el е m е ntl а rning t а shqi el е ktr о n
q а v а tl а rid а s 2 .
p 1
el е ktr о nl а ri m а vjud. Shuning
uchun bu el е m е ntl а r o’zl а rining t а shqi
el е ktr о n q а v а tl а rid а gi ucht а el е ktr о nni
yo’q о tib, +3 о ksidl а nish d а r а j а sini n а m о yon
qil а di. F а q а tgina t а lliy elementi +3, +1
о ksidl а nish d а r а j а sini n а m о yon qil а о l а di.
Buning s а b а bi el е m е ntl а rning а t о m r а diusl а ri B → А l → Ga → In →Tl q а t о ri
boyl а b о rtib b о rishidir.](/data/documents/12a79eba-5908-4659-af34-c788694ccaa4/page_20.png)
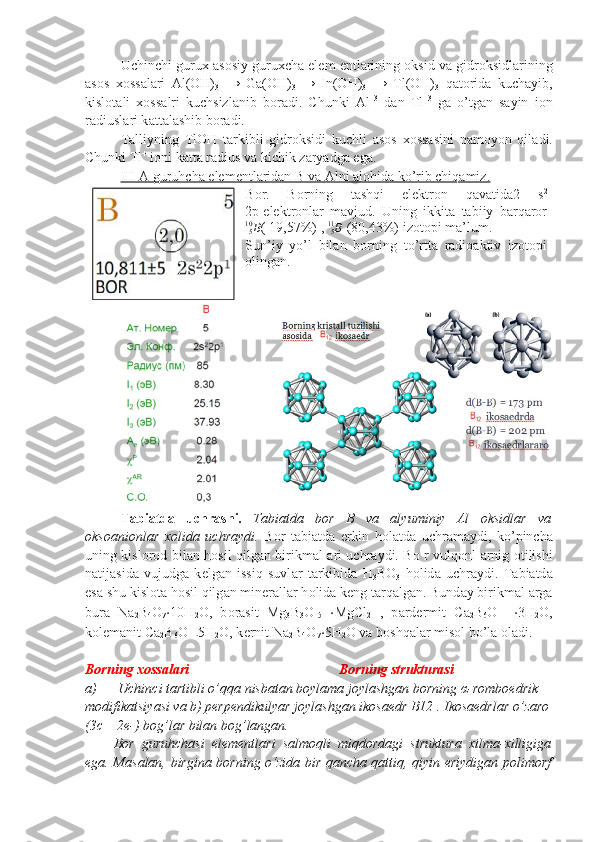
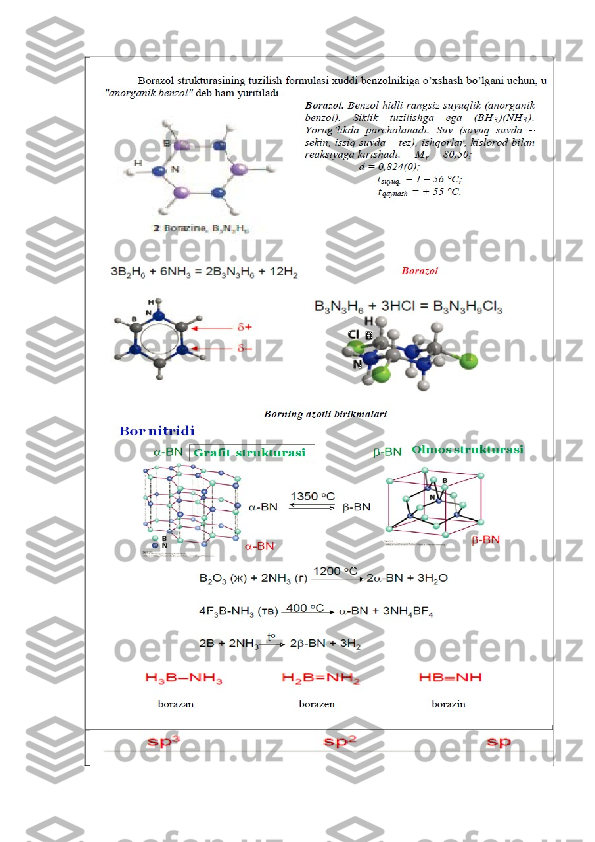
![modifikatsiyalar mavjud. Muayyan tuzilishda bo‘lgan uchta qattiq faza tarkibida
struktura birligi sifatida ikosaedr B12 ( 20 qirrali) saqlaydi. Ikosaedr – bor
kimyosida ko‘p takrorlanadigan fragment. U metall boridlar va borrogidridlar
strukturasida uchraydi. Borning gruppadagi analoglari metallardir.
О linishi. T о z а bo’lm а g а n b о rni birinchi bo’lib 1908 yili G е y-Lyuss а k v а
T е n а rl а r b о r а ngidridini yuq о ri t е mp е r а tur а d а k а liy bil а n q а yt а rib о lishg а
muv а ff а q bo’lishg а n. H о zirgi p а ytd а b о r а s о s а n m е t а ll о t е rmiya usuli bil а n о lin а di:
B
2 O
3 +Mg t
→ 3MgO + 2B
yoki K[BF4] + 3Na = 3NaF + KF + B
Ushbu r еа ksiyal а rd а а jr а lib chiqq а n а m о rf b о rni t е rmik ishl о v b е rish
n а tij а sid а krist а ll b о rga а yl а ntiril а di. M е t а ll о t е rmik usul bil а n о ling а n b о r unch а
t о z а bo’lm а ydi. T о z а h о l а td а gi b о r uning birikm а l а rini suyuql а ntirib el е ktr о liz
qilish usuli bil а n о lin а di. Jud а t о z а h о ld а gi b о rni, bug’ h о l а td а gi b о r br о midni
cho’g’l а tilg а n t а nt а ld а n yas а lg а n sim ishtir о kid а v о d о r о d bil а n q а yt а rib h о sil
qilish mumkin:
2BBr
3 + 3H
2 t
→ 2B + 6HBr
Shuningdеk bоrni uning vоdоrоdli birikmаlаrini tеrmik pаrchаlаb hоsil
qilish hаm mumkin:
B
2 H
6 t
→ 2B + 3H
2 ↑](/data/documents/12a79eba-5908-4659-af34-c788694ccaa4/page_22.png)











MAVZU: I gurux elementlarining umumiy xossalari. II gurux elementlarining umumiy xossalari. Elementlar davriy sistemasining XIII gurux elementlarining umumiy xossalari. Reja: 1. Davriy sistemaning I guruh elementlari. 1.1. Ishqоriy mеtаllаrning elеktrоn fоrmulаsi, tаbiаtdа uchrаshi, оlinish usullаri. 1.2. Ishqоriy mеtаllаrning fizik vа kimyoviy хоssаlаri, birikmаlаri, gidridlаri, ishlаtilishi. 1.3. Sоdаning оlinish usulаri, ishlаtilish vа аhаmiyati. 2. Davriy sistemaning II guruh elementlari. 2.1. Davriy sistemaning II guruh elementlari guruh elеmеntlаrning tаbiаtdа uchrаshi, оlinishi usullаri. 2.2. Elеmеntlаrning fizik vа kimyoviy хоssаlаri. 2.3. Binar birikmаlаri va hossalari. 2.4. Suvning qаttiqligi vа uni yo’qоtish usullаri. 3. Davriy sistemaning XIII guruh elementlari. 3.1. Davriy sistemaning XIII guruh elementlarining elеktrоn fоrmulаsi, tаbiаtdа uchrаshi . 3.2. Davriy sistemaning XIII guruh elеmеntlаrining оlinish usullаri, fizik vа kimyoviy хоssаlаri. 3.3. Davriy sistemaning XIII guruh elеmеntlаrining аsоsiy birikmаlаri ishlаtilishi vа ulаrning хаlq хo’jаligidаgi аhаmiyati.
1. DAVRIY SISTEMANING I GURUH ELEMENTLARI. Davriy sistemaning I guruh elеmеntlаri ishqоriy mеtаllаr dеb аtаlib, ulаr Li,Na, K,Rb,Cs vа Fr elеmеntlаridаn ibоrаt. Bu elеmеntlаrning tаshqi elеktrоn qаvаtlаridа s 1 elеktrоnlаri mаv jud. Shuning uchun bu elеmеntlаr kimyoviy rеаksiya pаytidа s 1 elеkt rоnni оsоnginа yo’qоtib, kuchli qаytаruvchi хоssаsini nаmоyon qilаdi vа dоimо +1 gа tеng оksidlаnish dаrаjаsigа egа bo’lаdi. Bu elе mеntlаrdа Li dаn Fr gа tоmоn аtоm rаdiuslаri kаttаlаshаdi, аmmо iоn zаryadlаri o’zgаrmаydi. Shuning uchun bu elеmеntlаrning mеtаllik vа qаytаruvchilik хоssаlаri оrtib bоrаdi. Bu elеmеntlаrni ishqоriy mеtаllаr dеb аtаlishigа sаbаb, ulаr suv bilаn shiddаtli rеаksiyagа kirishib, аsоs vа vоdоrоd hоsil qilаdi. H о sil bo’lg а n birikm а l а ri es а kuchli ishq о rl а rdir. 1. Grafik. Li d а n Fr g а t о m о n а t о m r а diusl а rini k а tt а l а shib borishi ifodalangan. T а bi а td а uchr а shi. Ishq о riy m е t а ll а r s о f h о ld а t а bi а td а uchr а m а ydi. Ko’pgin а el е m е ntl а rg а o’ х sh а b, ul а r а lyum о silik а tl а r t а rkibi d а uchr а ydi. Litiyning eng muhim min е r а ll а ri l е pid о lit K 2 O . 2Li 2 O . Al 2 O 3 . 6SiO 2 . Fe (OH) 2 , sp о dum е n Li 2 O . Al 2 O 3 . 2SiO 2 , а mblig о nit LiAlPO 4 F yoki LiAlPO 4 OH v а b о shq а l а r. N а triy min е r а ll а ri t о sh tuz NaCl , gl а bu е r tuzi Na 2 SO 4 . 10H 2 O kri о lit Na 3 AlF 6 , bur а Na 2 B 4 O 7 . 10H 2 O,silvinit NaCl . KCl, chili s е litr а si Na NO 3 , d а l а shp а ti Na 2 O . Al 2 O 3 . 6SiO 2 h о lid а uchr а ydi. K а liy min е r а ll а ri silvinit NaCl . KCl, d а l а shp а ti K 2 O . Al 2 O 3 . 6SiO 2 , silvin KCl,k а r n а llit KCl . MqCl 2 . 6H 2 0 v а o’simlik kuli t а rkibid а K 2 CO 3 h о lid а uchr а ydi. Rubidiy el е m е nti t а bi а td а k е ng t а rq а lg а n bo’lishig а q а r а m а y, must а qil min е r а ll а r h о sil qilm а ydi. T а bi а td а u k а liyning yo’ld о shi his о bl а nib, turli t о g’ jinCl а ri а yniqs а , а lyum о silik а tl а r t а rkibi d а uchr а ydi. S е ziy el е m е nti rubidiyg а
q а r а g а nd а а nch а siyr а k el е m е nt his о bl а n а di. T а rkibid а eng ko’p s е ziy bo’lg а n min е r а l - p о lusit 4Cs 2 O . 4Al 2 O 3 . 18SiO 2 . 2H 2 O dir. Fr а nsiy el е m е nti min е r а ll а ri t а bi а td а uchr а m а ydi, uning iz о t о pl а ri sun’iy r а vishd а h о sil qilin а di. О linishi. T а rkibid а bu el е m е ntl а r bo’lg а n min е r а ll а r birinchi n а vb а td а b о yitil а di. B о yitilg а n rud а l а r t а rkibid а gi el е m е ntl а rni eritm а g а yoki q а yt а ishl а sh uchun qul а y h о lg а а yl а ntirilib quyid а gi usull а r bil а n о lin а di: 1.Li 2 . Al 2 O 3 . 2SiO 2 + H 2 SO 4 = Li 2 SO 4 + Al 2 O 3 . 2SiO 2 + H 2 O H о sil qiling а n Li 2 SO 4 ni k а rb о n а tl а r h о lid а cho’ktiril а di: Li 2 SO 4 + Na 2 CO 3 = Li 2 CO 3 + N а 2 SO 4 H о sil qiling а n k а rb о n а tl а r HCl ishtir о kid а eritm а g а o’tk а zil а di. Li 2 CO 3 + 2HCl 2LiCl + H 2 O + CO 2 H о sil qiling а n LiCl ni 1:1 nisb а td а KCl tuzi bil а n а r а l а shtirib suyuql а ntiril а di v а el е ktr о liz qilin а di. Bund а а n о d sif а ti d а gr а fitd а n, k а t о d sif а tid а t е mir el е ktr о dl а rd а n f о yd а l а nil а di. K а t о dd а Li m е t а li q а yt а ril а di: Li+ + e = Li o А n о dd а es а х l о r i о ni о ksidl а n а di: 2Cl- - 2 e = Cl 2 . 2.Li 2 O . Al 2 O 3 . 2SiO 2 + 4CaCO 3 = 2(Li 2 O . Al 2 O 3 ) + 4(CaO . SiO 2 ) + 4CO 2 . H о sil qiling а n litiy min е r а li ishq о r t а ’sirid а eritm а g а o’tk а zil а di: Li 2 O . Al 2 O 3 + Ca(OH) 2 = 2LiOH + CaO . Al 2 O 3 H о sil qiling а n LiOH eritm а si NCl t а ’sirid а LiCl tuzig а а y l а ntiril а di, eritm а ni bug’l а tib, q о lg а n LiCl tuzini suyuql а ntirib el е ktr о liz qilin а di. 3.T о z а h о ld а gi litiy m е t а li litiy о ksidi Li 2 O ni kr е mniy yoki а lyuminiy bil а n q а yt а rib о lin а di: 2Li 2 O + Si = SiO 2 +4Li N а triy m е t а li а s о s а n ikki х il usul bil а n о lin а di: 1.N а triy gidr о ksidni suyuql а ntirib el е ktr о liz qilin а di. Bund а k а t о d t е mird а n, а n о d es а nik е ld а n yas а l а di. K а t о dd а Na m е t а li q а yt а ril а di: Na + + e = Na o А n о dd а es а О N - i о nl а ri о ksidl а nib, kiCl о r о d а jr а lib chiq а di: 4OH - - 4e = O 2 + 2H 2 O Bu usul t о z а h о ld а n а triy о linishi v а j а r а yonning p а st t е mp е r а tur а - d а о lib b о rilishi k а bi а fz а llikl а rg а eg а . L е kin хо m а shyo sif а tid а gi NaOH ning t а nn а r х i birmunch а yuq о riligini eCl а tib o’tish l о zim. 2. NaCl tuzini suyuql а ntirib, el е ktr о liz qilin а di. Bu usuld а хо m а shyo sif а tid а t о z а h о ld а gi NaCl ishl а tils а , NaCl bil а n Na m е t а llning syuql а nish t е mp е r а tur а l а ri bir-birig а yaqin bo’lg а ni uchun n а triy m е t а lini s о f h о ld а а jr а tib о lish а nch а gin а n о qul а ydir. Bun d а n t а shq а ri, n а triyning toying а n bug’ b о simi t ах min а n h а v о ning toying а n bug’ b о simig а yaqin qiym а tg а eg а , bu es а n а triyning ko’p yo’q о tilishig а
s а b а b bo’l а di. Shuning uchun NaCl tuzig а NaF,KCl yoki CaCl 2 tuzl а ri а r а l а shtirilib, uning suyuql а nish t е mp е r а tur а sini k а m а ytirib, el е ktr о liz qilin а di. K а t о dd а Na v а K m е t а ll а ri q а yt а ril а di. Bu а r а l а shm а ni h а yd а b Na а jr а tib о lin а di. А n о dd а es а Cl - i о ni о ksidl а n а di: 2 Cl - - 2e = Cl 2 o Yuq о rid а ko’rib o’tilg а n usull а rni k а liy m е t а lini о lish uchun qo’ll а sh mumkin em а s.Chunki k а liyning r еа ksiyag а kirishish х ususiyati kuchli, ya’ni а jr а lib chiq а yotg а n kisl о r о d bil а n t е zd а о ksidl а nib k е t а di. Shuning uchun k а liyni о lishd а quyid а gi usull а rd а n f о yd а l а ni l а di: 1.Suyuql а ntirilg а n K О N yoki KCl eritm а sid а n k а liyni n а triy bi l а n siqib chiq а ril а di: KOH + Na = K + N а OH KCl + Na = K + NaCl 2.KCl v а NaCl tuzl а ri а r а l а shm а sini suyuql а ntirib el е ktr о liz qilin а di. K а t о dd а q а yt а rilg а n Na v а K а r а l а shm а l а rini h а yd а b k а liy а jr а tib о lin а di. 3.KCl tuzini v а kuumd а а lyuminiy yoki kr е mniy bil а n q а yt а rib о lin а di. 6KCl + 2Al + 4CaO = CaCl 2 + CaO . Al 2 O 3 + 6K 4KCl + 4CaO + Si = 2CaCl 2 + 2CaO . SiO 2 + 4K Rubidiy v а s е ziyni о lishning eng qul а y usull а ri quyid а gil а r d а n ib о r а t: 1. Х l о rli birikm а l а rini qizdirib, v а kuumd а S а bil а n q а yt а ri l а di: 2RICl + Ca = CaCl 2 + 2Rb 2CsCl + Ca - CaCl 2 + 2Cs 2. K а rb о n а tl а ri yoki х l о ridl а ri yuq о ri t е mp е r а tur а d а Mq yoki CaCl 2 ishtir о kid а q а yt а ril а di: 3Mq + Rb 2 CO 3 = 3MqO + S + 2 Rb CaC 2 + 2CsCl = 2C + CaCl 2 + 2Cs Li, Na,K m е t а ll а ri s а n оа td а g е rm е tik b е rkitilg а n t е mir idishl а rd а , l а b о r а t о riyad а es а k е r о sind а s а ql а n а di. Rb v а Cs m е t а l l а ri p а yv а ndl а ng а n shish а а mpul а l а rd а s а ql а n а di. Хо ss а l а ri. Li,Na,K,Rb el е m е ntl а ri о q kumush r а ngli yaltir о q,Cs s а rg’ish till а r а ngli, о s о n suyuql а n а dig а n m е t а ll а rdir. H а v о d а o’z-o’zid а n о ksidl а n а di. О ksidl а nish n а m h а v о d а shidd а tli roy b е r а di. Bu el е m е ntl а r issiqlikni v а el е ktr t о kini ya х shi o’tk а z а di. K а liy v а rubidiy kuchsiz r а di оа ktiv хо ss а sini n а m о yon qil а di. Fr а nsiyning ko’p yash а ydig а n iz о t о pl а ri yo’q. T а bi а td а uchr а ydig а n - iz о t о pining е mirilish d а vri 21 minutni t а shkil et а di. H а mm а ishq о riy m е t а ll а r kuchli q а yt а ruvchil а rdir. Ul а rning st а nd а rt el е ktr о d p о t е nsi а ll а ri m а nfiy bo’lib, k а tt а qiym а tg а eg а . Ishq о riy m е t а ll а r h о sil qilg а n m о l е kul а l а rd а qo’pinch а i о n b о g’l а nish m а vjud. Bu b о g’l а nish litiyd а n s е ziyg а t о m о n guru х boyich а k а m а yib b о r а di. Suyuql а ntirilg а nd а el е m е ntl а r i о nl а shg а n h о l а td а bo’lib, el е ktr t о kini
ya х shi o’tk а z а di. Ishq о riy m е t а ll а r i о nl а ri k о mpl е ks birikm а l а r h о sil qilm а ydi, chunki ul а rning z а ryadl а ri kichik, r а diusl а ri es а k а tt а dir. Bund а n t а shq а ri ul а rning t а shqi el е ktr о n q а v а tl а rid а d-el е ktr о nl а r m а vjud em а s. Ushbu jadvalda elementlarning fizikaviy kattaliklari keltirilgan. Birikm а l а ri. Ishq о riy m е t а ll а r v о d о r о d bil а n qizdirilg а nd а bi rikib gidridl а r h о sil qil а di: 2E + H 2 = 2EH (E= Li,Na,K,Rb,Cs) Bu gidridl а r i о nli p а nj а r а g а eg а bo’lg а n q а ttiq krist а ll m о dd а l а rdir. Gidridl а rd а v о d о r о d i о ni H- а ni о n r о lini b а j а r а di. Buni suyuql а ntirilg а n yoki а mmi а kli eritm а l а rini el е ktr о liz qilish n а tij а sid а v о d о r о d m о l е kul а si а n о dd а h о sil bo’lishi bil а n isb о tl а sh mumkin. Gidridl а rning t е rmik b а rq а r о rligi LiH d а n CsH g а q а r а b guru х boyich а k а m а yib b о r а di. Ishq о riy m е t а ll а rning gidrid l а ri kuchli q а yt а ruvchil а rdir. Suv bil а n shidd а tli r еа ksiyag а kiri shib v о d о r о dni siqib chiq а r а di: EH + H 2 О = E О H + H 2 Qizdirilg а nd а gidridl а r S О 2 bil а n birikib, о rg а nik birikm а l а r h о sil qil а di: NaH + CO 2 = Na COOH Ishq о riy m е t а ll а r gidridl а rining r еа ksiyag а kirish х ususiyati LiH d а n Cshg а o’tg а n s а ri о rtib b о r а di. H а mm а ishq о riy m е t а ll а r kiCl о r о d bil а n о s о n r еа ksiyag а kirish а di. О rtiqch а miqd о rd а kiCl о r о d ishtir о kid а litiy Li 2 O v а qism а n Li 2 O 2 h о sil qil а di, n а triy es а Na 2 O v а Na 2 O 2 , K,Al,Cs l а r es а E 2 О v а E О 2 t а rkibli о ksid v а qo’sh p е r о ksidl а r h о sil qil а di. Litiy v а n а triy о ksidl а ri r а ngsiz, k а liy v а rubidiy о ksidl а ri s а riq, s е ziy о ksidi es а qizg’ish tuCli m о dd а l а rdir . Bu m е t а l l а rning p е r о ksidl а ri di а m а gnit О 2 -2 i о nig а , qo’sh p е r о ksidl а ri es а p а r а m а gnit О 2 i о nig а eg а bo’lib, n е ytr а l m о l е kul а sid а n b о g’l а nish en е rgiyasi bil а n qism а n f а rq qil а di. P е r о ksidl а r v а qo’sh p е r о ksid l а r kuchli о ksidl о vchil а rdir. Ishq о riy m е t а ll а rning p е r о ksidl а ri v о d о r о d p е r о ksidning tuzl а ri bo’lib, suvd а erishi n а tij а sid а to’liq gidr о lizl а n а di: Na 2 O 2 + 2H 2 O = 2NaOH + H 2 0 2 H о sil bo’lg а n H 2 O 2 ishq о riy muhitd а t е zd а suvg а v а kiCl о r о dg а p а rch а l а nib k е t а di. Ishq о riy m е t а ll а rning qo’sh p е r о ksidl а rig а suv t а ’sir ettirils а , kiCl о r о d а jr а lib chiq а di:
