Ammiakning xususiyatlari, ishlab chiqarish asoslari, ammiak sintezi qurulmalari


















O‘ZBEKISTON RESPUBLIKASI OLIY VA O‘RTA MAXSUS TA’LIM VAZIRLIGI SHAROF RASHIDOV NOMIDAGI SAMARQAND DAVLAT UNIVERSITETI Mavzu: Ammiakning xususiyatlari, ishlab chiqarish asoslari, ammiak sintezi qurulmalari
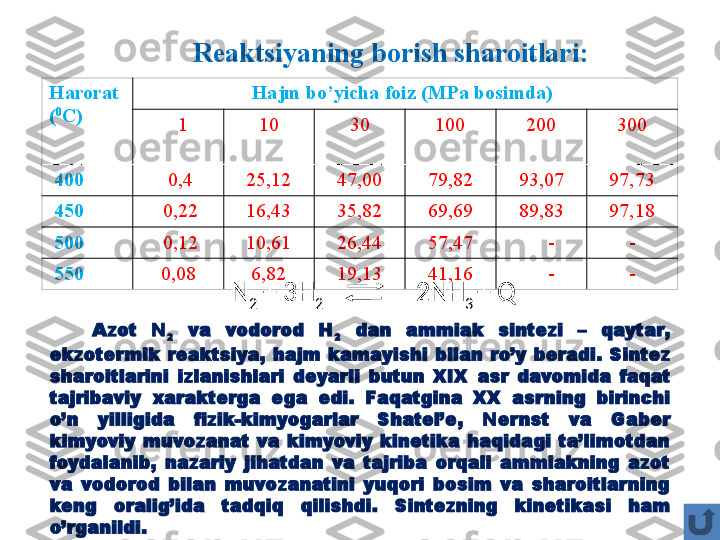
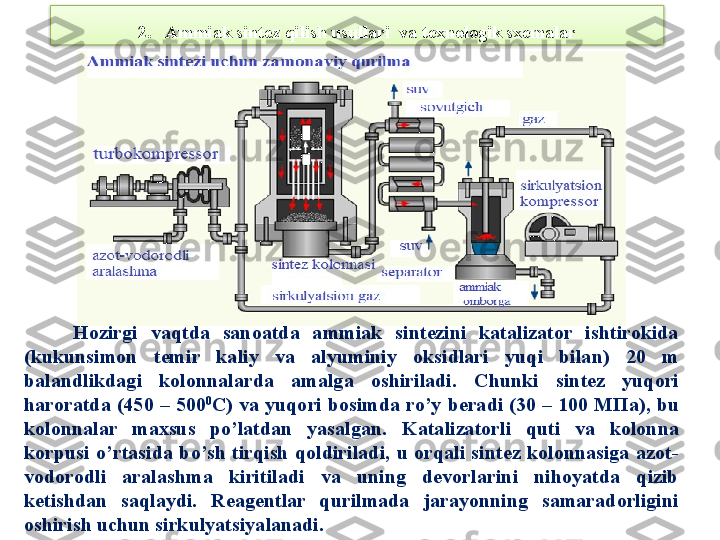
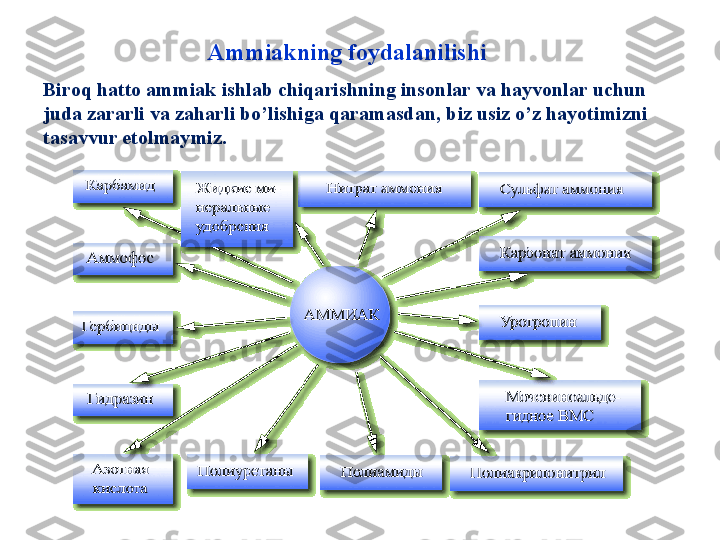
Mavzu rejasi: 1. Ammiak sentezida ishlatiladigan xomashyolar va ularni olish usullari a) Azotning xomashyo manbalari 2. Ammiak sentez qilish usullari va texnologik sxemalar 3. Ammiak sint е z qilish sanoatining t е xnika-iqtisodiy ko’rsatkichlari 4. Ammiakning ishlatilishi
Ammiak — NH 3 , vodorod nitrid , normal sharoitda — o’tkir o’ziga xos hidli rangsiz gaz ( nashatir spirti hidi ), havodan deyarli ikki marta engil , juda zaharli . Eruvchanligi NH 3 suvda nihoyatda katta - 1200 hajm atrofida (0 °C da ) yoki 700 hajm (20 °C da ) bir hajm suvda . М (NH 3 ) = 17 g / mol Nashatir spirti – ammiakning 10%- li suvli eritmasi
Ammiak sentezida asosiy xomashyolar azot va vodorod hisoblanadi. Ammiak sentezida toza holatdagi azot va vodorod gazlari k е rak.1. Ammiak sentezida ishlatiladigan xomashyolar va ularni olish usullari Azot tabiatda erkin holda va birikmalar ko’rinishida bo’ladi. Azotning asosiy qismi atmosferada ( massa bo’yicha 75,6 % ) erkin holda bo’ladi. Birikmalar shaklida esa yer po’stlog’ining 0,4 % ini ( massa bo’yicha ) azot tashkil etadi. U turli organik moddalar tarkibida, hayvonlar va o’simliklar tarkibida uchraydi. Anorganik birikmalar shaklida azot kam uchraydi. Uning nartiyli tuzi (Chili selitrasi ) Chilida va Janubiy Afrikada, kaliyli selitrasi ( Hind selitrasi ) esa Hindistonda topilgan. Ma’lum miqdor ammoniy sulfat tuzi ko’mirni ko’kslashdan olinadi. a) Azotning xomashyo manbalari
1. Ammiak sentezida ishlatiladigan xomashyolar va ularni olish usullari Azot havoni qattiq sovitish yo’li bilan olinadi. Ma’lumki, hamma gazlar katta bosim ostida siqilganda yoki sovitilganda suyuqlikka aylanadi. Xuddi shunga o’xshash, havo ham qattiq sovitilganda suyuqlikka aylanadi; so’ngra suyuqlikni undagi moddalarning qaynash t е mp е raturasiga ko’ra xaydab, azot bilan kislorodga ajratiladi. Azot kislorodga nisbatan past t е mp е raturada qaynaydi, ya’ni t° qayn N 2 =- 195,7°C va t° qayn O 2 = -183°C. Shuning uchun suyuqlangan azot bilan kislorod aralashmasi xaydalganda, avvalo azot, sungra kislorod bug’lanadi (yoki kislorodni suyuq xolda qoldirishimiz mumkin). Shunday qilib, biz xavodan azotni ajratib oldik. Bu jarayon natijasida olingan toza kislorod yoki kislorod bilan boyitilgan xavo m е tallurgiya, kimyo va sanoatning boshqa tarmoqlarida k е ng qo’llaniladi. Toza azot olish usuli:
