LYCIUM DEPRESSUM MEVASINING ALKOLOID TARKIBINI O‘RGANISH



![4
II. ADABIYOTLAR SHARHI
2.1. Alkaloidlar tasnif i
Hozirgi vaqtda 10000 ga yaqin alkaloidlar turi bo‘lib, ulardan 4000 tasining
tuzilishi isbotlangan [1-3]. Bunday ko‘p miqdor alkaloidlarni turlicha sinflashga
sabab bo‘lmoqda. Alkaloidlarni sinflashning bir qancha prinsiplari bo‘lib, ularning
ayrimlari quyida keltirilgan.
Alkaloidlarni farmakologik xossalariga ko‘ra klassifikatsiyalashda ularning
organizmga ta’siri asos qilib olinadi:
- narkotik alkaloidlar;
- mahalliy og‘riqsizlantiruvchi alkaloidlar;
- spazmalitik alkaloidlar;
- kurarega o‘xshash (farmakologik ta’siri) ta’sirga ega alkaloidlar.
Botanik klassifikatsiyalash asosida esa o‘simlik oilalari asos qilib olinib, ulardan
ajratib olingan alkaloidlar birgalikda guruhlanadi:
- tamakidoshlar alkaloidlari;
- lolaguldoshlar alkaloidlari;
- sporinlar alkaloidlari.
Bu klassifikatsiyalar alkaloidlarning kimyoviy tuzilishini e’tiborga olmaydi.
Angliyalik olim Xegnauer biogenetik klassifikatsiyani taklif qildi. Bu
klassifikatsiyada alkaloidlarning biosintez yo‘liga e’tibor qaratiladi, ya’ni alkaloidlar
hosil bo‘lishida ishtirok etayotgan aminokislotalar asosiy hisoblanadi. Shunga ko‘ra
quyidagi alkaoidlar guruhlari ajratiladi:
- triptofan alkaloidlari;
- fenilalanin alkaloidlari.
1910-yilda E.Vintershteyn va T.Trir alkaloidlar to‘g‘risidagi zamonaviy
tushunchalarni izohlab, haqiqiy alkaloid bo‘lishi uchun quyidagi to‘rt shart bajarilishi
kerak deb e’tirof etadilar.
1. Azot atomi geterosiklik halqa tarkibida bo‘lishi kerak;
2. Birikma murakkab molekulyar strukturaga ega bo‘lishi kerak;](/data/documents/c49d4c8e-34dd-4933-848d-80060630b84f/page_4.png)
![5
3. Ular albatta farmakologik faol bo‘lishi kerak;
4. O‘simlik tarkibida bo‘lishi kerak .
Lekin barcha alakaloidlar ham bu talablarga javob bera olmaydi. Kolxitsin,
piperin kabi alkaloidlar asos xarakteriga ega emas. Kolxitsin meskalin va
feniletilamin singarilar geterosiklik birikma hisoblanmaydi [4].
Professor V.S.Sokolov [5] alkaloidlar uchraydigan o‘simlik oilalarini hisobga
olib, alkaloid saqlagan o‘simliklarni 3 guruhga ajratadi:
1 guruh oilalar – 20% dan kam bo‘lmagan alkaloid saqlagan o‘simliklar oilalari.
Bu oilalarni Sokolov alkaloidlarga boy oilalar deb atadi.
2 guruh oilalar – 10% dan 20 % gacha alkaloid saqlagan o‘simliklar oilalari. Bu
oilalar – o‘rtacha alkaloidli hisoblanadi.
3 guruh oilalar – 1% dan 10 % gacha alkaloid saqlagan o‘simliklar oilalari.
Bunday oilalar –kam alkaloidli hisoblanadi.
Hozirgi vaqtada molekulada azot atomining joylashishiga qarab alkaloidlar
quyidagi guruhlarga ajratiladi:
1. Haqiqiy alkaloidlar – azot atomi tutgan geterosiklik birikmalar va
aminokislotalardan tashkil topgan birikmalar (giosiamin, kofein, platifillin).
2. Protoalkaloidlar – yon zanjirida azot saqlagan alifatik birikmalar va
aminokislotalardan tashkil topgan birikmalar (efedrin, kapsaitsin).
3. Psevdoalkaloidlar – terpen va steroid tabiatli azot saqlagan birikmalar
(sоlаsоdin).
Ko‘pincha farmakognoziyada akad.A.P.Orexov taklif qilgan kimyoviy
klassifikatsiyadan foydalaniladi.
Bu klassifikatsiya asosida asosan azot saqlagan geterosiklik tuzilishli
alkaloidning kimyoviy tuzilishi yotadi.](/data/documents/c49d4c8e-34dd-4933-848d-80060630b84f/page_5.png)
![6
A.P.Orexov klassifikatsiyasida alkaloid molekulasi tarkibidagi geterosiklning
tuzilishiga e’tibor qaratiladi. Bu klassifikatsiyaga asosan alkaloidlar quyidagi
guruhlarga ajratiladi [ 4-6 ]:
Jadval №1
1. Pirrolidin
2. Piperidin
3. Piridin
4. Pirrolizidin
5.Х inolizidin
6. Х inolin 7. Izoxinolin
8. Хinazolin
9. Indol
10.Тropan
11.Digidroindol
12. Imidazol 13. Аkridin
14. Purin
15. Steroidli alkaloidlar
16. Terpeniod alkaloidlari
17. Geterohalqasiz alkaloidlar
18.Tuzilishi aniqlanmagan alkaloidlar.
Ko‘pchilik tabiiy birikmalarga nisbatan alkaloidlar turli-tuman tuzilishga ega
birikmalar hisoblanadi. Shuning uchun ham alkaoidlarni tasniflashda aniq bir ustun
klassifikatsiya mavjud emas.
Hozirda alkaloidlarning zamonaviy klassifikatsiyasidan keng foydalaniladi. Bu
klassifaksiyada alkaloidlar uglerod skletining tuzilishi yoki biogenetik kelib
chiqishidagi asosiy birikmaga asoslaniladi.
Quyida alkaloidlarni 28 xil strukturali turlarini keltirdik. Ularning ichida
izoxinolin guruhiga tegishli 26 xil, xinolinga tegishli 4 xil, indolga tegishli 7 xil
guruhchalar ham kiritilgan [1-4,7].
Alkaloidlar asosan quyidagi turlarga bo‘linadi: (jadval 2)
Jadval №2
ALKALOIDLARNING ASOSIY SINFLARI
1. Pirrolidin hosilalari
11. Tiazol hosilalari 21. Putressin hosilalari
(poliaminli alkaloidlar)
2. Tropan hosilalari
12. Xinazolin hosilalari 22. Spermidin hosilalari](/data/documents/c49d4c8e-34dd-4933-848d-80060630b84f/page_6.png)

![9
birikmalar LPS tomonidan 30 mkM da qo'zg'atilgan RAW 264,7 hujayralarining NO
chiqarilishini ingibirlashi mumkin [8].
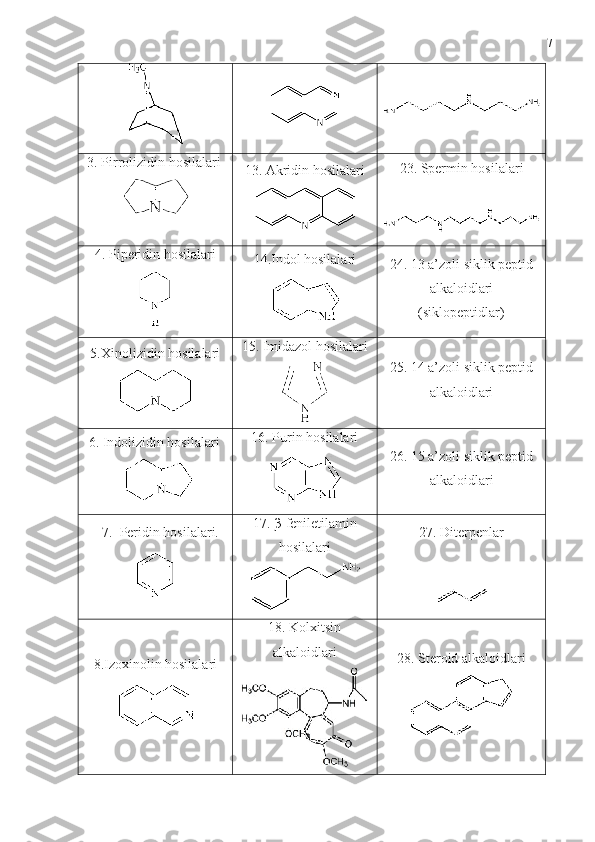
1000 dan ortiq vakillari o‘simliklardan ajratib olingan bo‘lib, shundan 250 ga
yaqini dimer va trimer ko‘rinishdagilarga tegishli. Dimer alkaloidlari efir bog‘lari
bilan bog‘langan bo‘lib, ularga glikoalkaloidlar ham kiradi. Gliko alkaloidlarda
aglikon qismi aporfin yoki benzilizoxinolin hisoblanadi. Izoxinolin qatori
alkaloidlarning ko‘p vakillari tabiiy biogenetik jarayonlarda hosil bo‘ladi. Misol
tariqasida o‘simliklarda dofamin 3,4–digidroksifenilpirouzum kislotasi 1 (tirozindan
hosil bo‘lgan) bilan kondensatsiyalanishidan 1-benzilizoxinolin 2 hosil bo‘ladi.
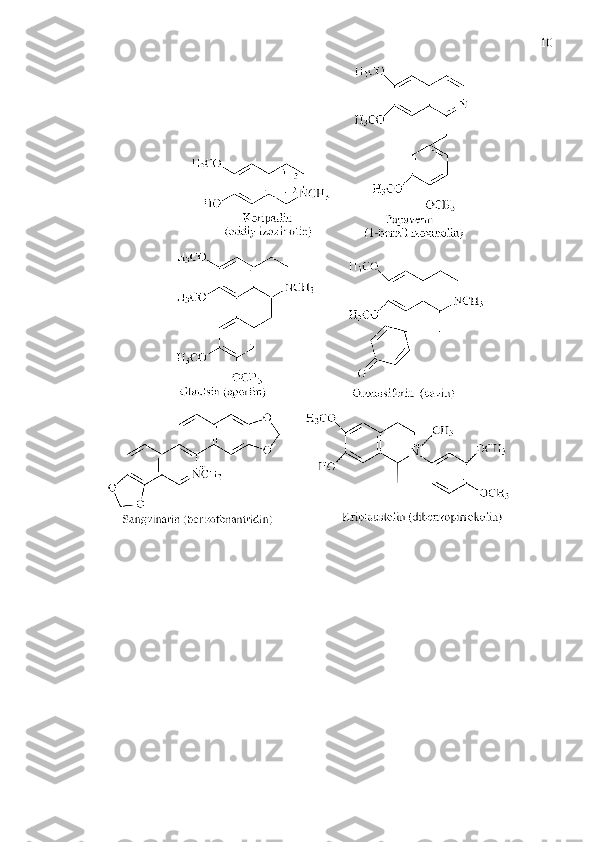
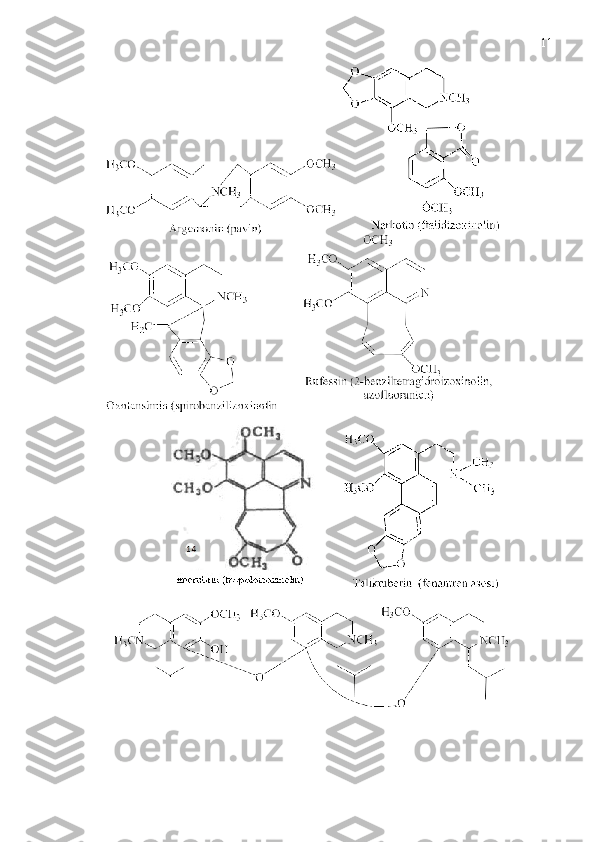
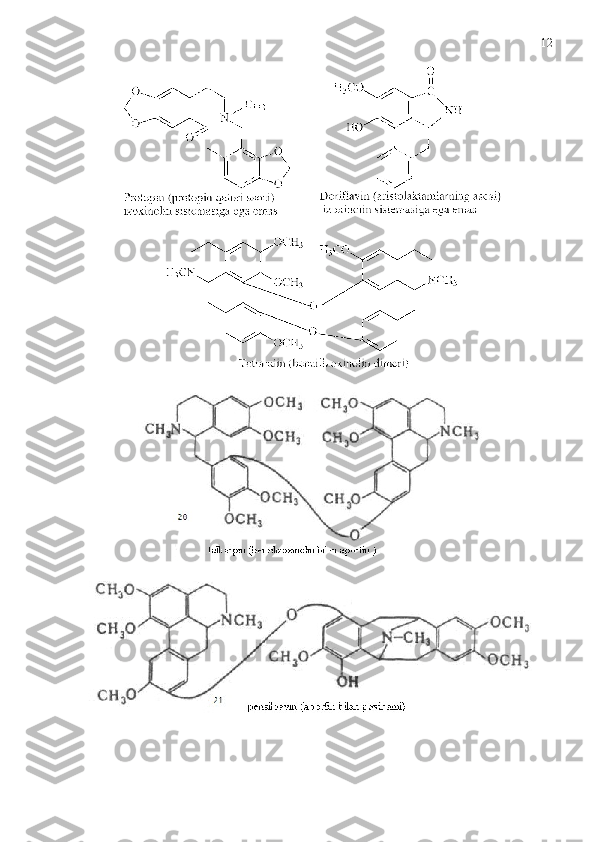
Quyida izoxinolin qatori alkaloidlarining bir nechtasini struktura tuzilishlari
bilan keltirdik [10,11].](/data/documents/c49d4c8e-34dd-4933-848d-80060630b84f/page_9.png)
![13
2. 3 . Lycium turkumining kimyoviy tarkibi
Ko‘p sonli dori vositalarining 40% ga yaqini tabiiy birikmalar tarkibiga kiradi.
Alkaloidlar (asosan izoxinolin alkaloidlari) esa dori moddalarning muhim sinfi
sifatida juda keng farmakologik ta’sirga ega birikmalar hisoblanadi. Tabiiy
birikmalarni kimyoviy modifikatsiyalash ularning spetsifik biologik faolligini
oshirish bilan birga, yangi biologik xossali birikmalar sinteziga ham sharoit yaratadi.
So‘nggi paytlarda bu jinsning kimyosiga qiziqishning ortishi 214 ta birikmani
ajratib olish va aniqlashga olib keldi. Ular alkaloidlar, amidlar, peptidlar,
flavonoidlar, kumarinlar, lignanlar, terpenoidlar, sterollar va steroidlar, organik
kislotalar va ularning hosilalari, polisaxaridlar, karotinoidlar, ozuqa moddalari va efir
moylarining turli sinflariga tegishli. Ularning tuzilmalari quyida ko ‘ rsatilgan va
ularning nomlari va tegishli o‘simlik manbalari j advalda to‘plangan.
T/r Birikma sinfi va nomi Manba O‘simlik qismi Adabiyot
Nortrop alkaloidlar
1 Kalistegin A3 L.chinense ildiz qobig‘i [3]
2 Kalistegin A5 L.chinense ildiz qobig‘i [3]
3 Kalistegin A6 L.chinense ildiz qobig‘i [3]
4 Kalistegin A7 L.chinense ildiz qobig‘i [3]
5 Kalistegin B1 L.chinense ildiz qobig‘i [3]
6 Kalistegin B2 L.chinense ildiz qobig‘i [3]
7 Kalistegin B3 L.chinense ildiz qobig‘i [3]
8 Kalistegin B4 L.chinense ildiz qobig‘i [3]
9 Kalistegin B5 L.chinense ildiz qobig‘i [3]
10 Kalistegin C1 L.chinense ildiz qobig‘i [3]
11 Kalistegin C2 L.chinense ildiz qobig‘i [3]
12 Kalistegin N1 L.chinense ildiz qobig‘i [3]
13 N-metilkalistegin B2 L.chinense ildiz qobig‘i [3]
14 N-metilKalistegin C1 L.chinense ildiz qobig‘i [3]](/data/documents/c49d4c8e-34dd-4933-848d-80060630b84f/page_13.png)
![14
Tropan alkaloidlari
15 Atropin L.halimifolium barg, ildiz [4]
16 Skopolamin L.barbarum meva, ildiz [5], [6]
17 Giosiamin L.halimifolium barg, ildiz [4]
Piperidin alkaloidlari
18 Fagomin L.chinense ildiz qobig‘i [3]
19 6-Deoksifagomin L.chinense ildiz qobig‘i [3]
Pirrol hosilalari
20 4-[2-Formil-5-
(gidroksimetil)1H-pirrol-
1-il] butan kislota L.chinense meva [7]
21 4-[2-Formil-5-
(metoksimetil)1H-pirrol-1-
il] butan kislota L.chinense meva [7]
22 Metil4-[2-formil-5-
(metoksimetil)-1H-pirrol-
1-il] butanoat L.chinense meva [7]
Pirrolidin alkaloidlari
23 Alkaloid I L.chinense ildiz qobig‘i [8]
24 Alkaloid II L.chinense ildiz qobig‘i [8]
Spermin alkaloidlari
25 Kukoamin A L.chinense ildiz qobig‘i [9]
26 Kukoamin B L.chinense ildiz qobig‘i [10]
Imidazol alkaloidlari
27 N α
-[(Z)-Sinnamoil]
gistamin L.cestroids bargi [11]
28 N α
-[(E)-Sinnamoil]
gistamin L.cestroids
L.barbarum bargi [11]
29 (Z)-Kuazibisiklik L.cestroids bargi [11]
30 (E)-Kuazibisiklik L.cestroids bargi [11]
31 N α
-[(Z)-Sinnamoil]-N
1 -
metilgistamin L.cestroids bargi [11]
32 N α
-[(E)-Sinnamoil]-N
1 -
metilgistamin L.cestroids bargi [11]](/data/documents/c49d4c8e-34dd-4933-848d-80060630b84f/page_14.png)

![16
Agar formaldegiddan boshqa aldegid olinsa, birinchi uglerodi o‘rinbosarga ega
bo‘lgan tetragidroizoxinolin hosilalari 10 olinadi [12].
Sintetik reaksiyalar natijalari reagentlar tabiatiga va tajriba sharoitlariga bog‘liq
bo‘ladi. Fiziologik faol tabiiy birikmalar modifikatsiyalarini izlash yuqori faollikka
ega yangi preparatlar sintezi uchun keng yo‘l ochadi hamda fiziologik faollik va
birikmaning kimyoviy tuzilishi orasidagi bog‘liqlikni o‘rnatishga imkon beradi.
Yadroda elektronoakseptor o‘rinbosar bo‘lganda hatto juda qattiq sharoitlarda
ham faqat quyidagi sikllanish mahsuloti hosil bo‘ladi:
Yoki Bishler-Napiralskiy reaksiyasida dastlabki modda sifatida feniletilamin 6
olinib, ikkinchi modda sifatida kislota xlor angidridlari olinsa 1-almashingan
izoxinolin hosilalari olinadi. Feniletilaminni atsillash va siklizasiyalanish
reaksiyalari Luis kislotalari ishtirokida amalga oshadi va 3,4,-digidroizoxinolin
hosilasi 21, 22 olinadi. Benzol halqasida elektronoakseptor guruh bo‘lganda bu
reaksiya juda kam unum bilan boradi.
Bishler–Napiralskiy reaksiyasidagi POCl
3 reaksiyani borishiga sharoit yaratadi
va juda oson degidratlanishni ta’minlaydi.](/data/documents/c49d4c8e-34dd-4933-848d-80060630b84f/page_16.png)
![17
Katalizator sifatida SnCl
4 dan foydalanilganda, aromatik yadroda benzol
halaqsini passivlashtiruvchi galogen atomi bo‘lsa ham sikllanish amalga oshadi [13].
Bunda SnCl
4 Luis kislotasi vazifasini bajaradi va π–aromatik sistemani faollashtiradi.
Sikllanish usulining yana bir ko‘rinishi Ritter reaksiyasi hisoblanadi. Bu reaksiya
izoxinolin halqasi sikllashda avvaldan ma’lum bo‘lsada, faqatgina keyingi yillarda
keng ishlatila boshlandi [14-20]. Bu usul qator qulayliklarga ega bo‘lsada, Bishler-
Napiralsiy reaksiyasi sharoitida qiyin amalga oshiriladi. Ayrim hollarda 3,3-dialkil va
3-spiroannel izoxinolinlarni olishda ishlatiladi [14,21]. Bu usulda benzol [ f ]
izoxinolinlar ham sintez qilingan [18,22]. Mualliflar [23] Ritter reaksiyasi bo‘yicha
izoxinolin halqasi sikllanishini amalga oshirishda nitrilli birikma sifatida sianid
kislotadan foydalanishgan [24]:
Ritter reaksiyasi bo‘yicha sikllanish reaksiyasi mexanizmini o‘rganish shuni
ko‘rsatdiki, reaksiyada kam sonli intermediatlardan foydalanish imkoniyati mavjud.
Mualliflar [25] shunday xossalarni izlash natijasi sifatida o‘rnatgan korrelyatsiyasida
reaksiya nitril tuzlari orqali borishi ta’kidlandi. Mualliflarning [26] ko‘rsatishicha,
sikllanishda nafaqat karbinollar, balki, ketonlar masalan, 3,4-dimetoksifenilaseton
reaksiya intermediati sifatida (nitril ioni ham) ham ishtirok etishi mumkin. 3,4-
digidroizoxinolinlar sintezining boshqa usullarida o‘rinbosarsiz benzol halqasi
birinchi holatiga birikishi keltirilgan. Ko‘pincha ushbu reaksiya 2-
galogenetilbenzaldegidning 23 ammiak bilan ta’siri holida ham beriladi [27,28].](/data/documents/c49d4c8e-34dd-4933-848d-80060630b84f/page_17.png)
![18
Aynan shunday reaksiya natijasida 20 o
C da yuqori unum bilan 24 mahsulot hosil
bo‘ladi:
Ichki molekulyar sikllanishda reaksiya aldegid guruhi hisobiga oson boradi
(metilen xlorid bilan qizdirish orqali) [ 29 ].
Bishler-Napiralskiy va Ritterning elektrofil almashinish mexanizmi bilan
boruvchi reaksiyalarida 7,8-dialkoksiizoxinolinlarni olib bo‘lmaydi, chunki benzol
halqasidagi yo‘naltirish sikllanishga imkon bermaydi. Mualliflar [30] metillangan β–
feniletilamindan yangi regioselektiv usulda izoxinolin olishni ishlab chiqdilar. Bunda
boshlang‘ich mahsulot gomoveratrilamindagi azot atomi trimetilxlor silan bilan
himoyalanadi. So‘ngra n- butillitiy bilan ishlanib, litiy organik intermediat 25 ga
aylantiriladi. Hosil bo‘lgan mahsulot DMFA bilan ta’sirlashib 26 mahsulotni hosil
qiladi.
Bishler-Napiralskiy bo‘yicha sintezlarda aromatik yadrodagi akseptor o‘rinbosar
hisobiga uning faolligi kamayadi va boshqa elektrofil reaksiyalar bormaydi. [ 31 ]
ishda 3,4-digidroizoxinolin hosilasini olishda 7 holatda triftor metil qoldig‘i saqlagan
birikmadan foydalaniladi. 27 birikma FeCl
3 va oksasilxlorid ishtirokida qayta ishlab,
kondensatsiyalashdan oksazolidin-4,5-dion 28 olinadi. Uni qizdirib, destruksiyalab
imin 29 hosil qilinadi:](/data/documents/c49d4c8e-34dd-4933-848d-80060630b84f/page_18.png)
![19
Izoxinolin hosilalari sintezida Pikte-Shplenger usuli katta ahamiyatga ega
hisoblanadi. Pikte-Shplenger reaksiyasida sikllanish Bishler-Napiralskiy usuliga
o‘xshash bo‘lib, dastlab iminlar hosil bo‘ladi. Iminlar aldegidlarning β -o‘rinbosarlar
bilan reaksiyasidan hosil bo‘ladi. Sikllanish reaksiyasi juda oson, ba’zan fiziologik
sharoitlarda ham (pH muhiti, temperatura, reagentlar konsentratsiyasi) borib,
gidrogenlangan izoxinolin hosilasi 32 yuqori unumda hosil bo‘ladi.
Odatda bu reaksiyalar suvli eritmada 100 o
C atrofida xlorid kislota ishtirokida
olib boriladi (juda kam hollarda sulfat, sirka va chumoli kislotalar ishlatiladi). Bu
reaksiyalarda qoidaga asosan formaldegid, sirka aldegidi va almashingan
benzaldegidlar va 2-fenil asetaldegidlardan (ko‘pchilik hollarda boshlang‘ich aldegid
beqaror bo‘lsa, uning o‘rniga asetal yoki enol efirlar ishlatiladi) foydalaniladi. Aminli
komponent sifatida esa 2-geteril yoki 2-feniletilaminlar, almashinmagan yoki halqada
alkoksi va gidroksiguruhlarga ega bo’lgan vakillari ishlatiladi. Alkoksi guruhning
bo‘lishi siklizasiyani osonlashtiradi, ya’ni, para holatda faollashgan guruhga
yuboriladi. Halqada gidroksil guruhning bo‘lishi ya’ni, fenol gidroksilining bo‘lishi,
benzol halqasini yanada faollashtiradi. Bunda reaksiya 25-40 o
C da рН = 4-8 gacha
bo‘lgan hollarda faqat aldegidlar bilan emas, ketonlar bilan, -oksikislotalar bilan
ham juda oson orto- va para- holatlarda (gidroksil guruhiga nisbatan) amalga
oshadi[32].](/data/documents/c49d4c8e-34dd-4933-848d-80060630b84f/page_19.png)


![22
almashingan izoxinolinlar bo‘ladi. Aldegidlar o‘rinbosarga nisbatan orto- va para-
holatda, ketonlar esa juda kam unum bilan izoxinolinlar hosil qiladi yoki umuman
reaksiyaga kirishmaydi.
Izoxinolin skletini sintez qilib olishda asetofenonni α-aminoasetasetal bilan
kondensatsiyalanishdan ham foydalanilgan. Keyingi bosqichda olingan Shiff asoslari
58 kislotali sharoitda siklizatsiya reaksiyasiga kirishadi [33-35]. Bu reaksiyalar
ketonlar bilan qiyinroq, aldegidlar bilan osonroq boradi. Aromatik aldegid va
ketonlar bilan jarayon ancha yengil kechadi.
Aromatik aldegidlar to‘g‘ridan-to‘g‘ri aminoasitallar bilan kondensatsiyalandi,
hosil bo‘lgan Shiff asoslari kislotali katalizator ishtirokida sikllanadi.](/data/documents/c49d4c8e-34dd-4933-848d-80060630b84f/page_22.png)

![24
2. 4 . Lycium turkumi o ptik faol alkaloidlari
Optik faol izoxinolin hosilalarini olishda С4-С4α bog‘ning tutashishi asosiy
usul hisoblanib, bu juda xilma-xil sterioselektiv sintez usullarini o‘z ichiga oladi.
Rozvadovskiy [55] iminga 99 metillitiyning birikishi xiral oksazolin 100
ishtirokidagi tipik Pomeran-Frich reaksiyasidan foydalanadi. Reaksiya natijasida
57%(46% ее) unum bilan (–)-salsolidin 101 , 79% (36% ее) unum bilan (–)-
karnegin 103 oladi.
Xi
ral ligand sifatida oksazolin 104 dan foydalanilgan. Umumiy formulasi:
Ispan olimlari [56] (3S, 4S)-6,7-dimetoksi-4-gidroksi-3- fenil-TIQ 101 sintezi
uchun optik faol imin 105 veratriviy аldegid (S)–fenilglitsin kondensatsiyasidan
foydalanishgan. Bu holatda imin E- konfiguratsiyaga ega.
NaBH
4 bilan qaytarish natijasida 106 hosil bo‘ladi, uni HCHO qayta ishlash
natijasida oksozolidin 106' hosil bo‘ladi. Halqaning ochilishi bilan 107 hosil bo‘ladi,](/data/documents/c49d4c8e-34dd-4933-848d-80060630b84f/page_24.png)
![25
u oksidlanib 107' , mahsulot aldegidgacha oksidlanib, kislotali sharoitda qayta
ishlanganda asosiy mahsulot 108 hosil bo‘ladi.
[57] mualliflar ancha qiziqarli tadqiqot o‘tkazishdi. Ular С4-С4α bog‘larni
tutashtirib, (-)-(R)-N-3,4-dimetoksibenzilxalostosinni 111 fenil halqasi bo‘yicha
Cr(CO)
3 kompleksiga bog‘lab (R,S)-hosila va xalostosindan olishdi. Toza birikma 4-
fenil-N-metil-TIQ 1 11 foydalanib, 20 o
С da 14% va -20 o
С da 54% unum bilan optik
faol TIQ 1 12 olinadi.
Mualliflar kuzatilayotgan diasteroselektivlikni tushuntirish uchun quyidagi
mexanizmi taklif etdilar:](/data/documents/c49d4c8e-34dd-4933-848d-80060630b84f/page_25.png)
![26
Reaksiya mahsulotining steriokimyoviy jihatdan tozaligi R-o‘rinbosarning
konfiguratsiyasi va uning hajmi bilan aniqlanadi. С1-С8α bog‘larning tutashishi
Bishler-Napiralskiy va Pikte-Shplenger reaksiyalari uchun xosdir.
( R )-( – )-lаudozin 125 sintezida Bishler-Napiralskiy reaksiyasidan foydalanilgan.
Bu sintezning (R)-( – )-glautsin 12 6 hosil qilish bosqichi juda muhimdir [53].](/data/documents/c49d4c8e-34dd-4933-848d-80060630b84f/page_26.png)
![27
S а lsolinol- 1- karbon kislotaaning 1 31 o‘ziga xos enentioselektiv sintezi [54] da
ifodalangan . Pirouzum kislotaning (+)-(1S,3S,4R)-mеntil efirining 128 dofamin 127
bilan reaksiyasidan 85% unum bilan diastereoizomerlar aralashmasi 129 56:44
nisbatda hosil bo‘ladi. Bu aralashmadan bitta izomerni 130 (de > 99%) ikki yoki uch
marta suvsiz metanolda (ИПС- MeOH) qayta kristallab olinadi. АсОН-kons.HCl
(1:1) gidrolizidan (-)-(R)- salsolinol-1 karbon kislota 1 31 olinadi.
(-)-sаlsolidin 101 alkaloidi sintezi Meyers tomonidan taklif etilgan [55]. U 2-
asetilgomoveratril kislotaning 132 (S)-fenilglitsinol bilan sintezidan kerakli
konfiguratsiyadagi bisiklik geterosikl 134 hosil qildi. So‘ngra olingan mahsulotni](/data/documents/c49d4c8e-34dd-4933-848d-80060630b84f/page_27.png)


![30
O‘simliklardan ajratib olingan alkaloidlarning soni 1500 yaqin [1,7,12]. Papaver,
Corydalis, Fumaria kabi o ‘ simlik oilalari izoxinolin qatori alkaloidlariga boy.
Tibbiyotda oddiy izoxinolin, fenilizoxinolin, benzilizoxinolin, diizoxinolin, aporfin
va boshqa guruhlarga tegishli alkaloidlar juda keng ishlatilmoqda. Misol tariqasida
ulardan morfin, kodein, papaverin, aporfin, glausin, sangvinarin, xeleritrin, α - β -
bikukulin, α - β -gidrastin va boshqalar [61,62].
Retikulin trombositlar agregatsiyasida kuchli ingibitor hisoblanadi. Berberin
va talifendin alkaloidlarining to‘rtlamchi tuzlari mikroorganizm va parazitlarga
qarshi (antiplazmotik va antiameb agent sifatida) kuchli antibiotik modda
hisoblanadi.](/data/documents/c49d4c8e-34dd-4933-848d-80060630b84f/page_30.png)
![31
Berberinning analogi besh a’zoli to‘rtlamchi alkaloidlar xeleritrin va fagaridin
kuchli sitostatiklar hisoblanadi. Bu moddalar ko‘krak hamda prostata bezlari rakini
davolashda ishlatiladi.
Kokkulin alkaloidi gipotenziv va ganglioblokator xossalarga ega. Noskanin
esa yo‘talga qarshi va balg‘am ko‘chiruvchi vosita sifatida qo‘llaniladi [63].
Ikkita izoxinolin fragmentiga ega bo‘lgan alkaloid dauritsin antiaritmik,
antigipotenziv va yallig‘lanishga qarshi kurashuvchi vosita sifatida ishlatiladi.
Dimer alkaloidlarining asosini 1-benzilizoxinolin yoki aporfin alkalodlari gidro yoki
degidro formalarida uchraydi. Meditsina nuqtai nazaridan bunday alkaloidlar og‘riqni](/data/documents/c49d4c8e-34dd-4933-848d-80060630b84f/page_31.png)
![32
qoldiruvchi, shamollashga qarshi, gipotenziv va sudirgiga qarshi kurashuvchi
vositalar sifatida ishlatiladi.
Tetrandrin
Talikarpin
Tetrandrin va talikarpin rakga qarshi aktivlikga ega bundan tashqari, ular har
xil tuberkulyoz bakteriya shtammlariga nisbatan tuberkulostatik ta’sirga ham ega
hisoblanadi [61,64].
O‘simliklarda izoxinolin alkaloidlari fenilalanin va tirozin asosida hosil bo’ladi
[5]. Izoxinolin qatori alkaloidlari ayrim guruhchalariga tegishli alkaloidlari bilan
mashhurdir.
Bеrbеrin bu sariq rangli alkaloid, oddiy barbaris tomirida, kanada sariq
tomirida (Hidrostis candehbis, po’stlog‘ida Xantoxylumolova heralis)da topilgan.
Bеrbеrin kuchsiz, optik faol bo‘lmagan moddadir. U suvda va spirtda eriydi, tuzlari
sariq rangga bo‘yalgan.
Emetin ipekakunani (Cephaelis ipecacuanha yoki Chephallis acuminata) asosiy
alkaloidi, P.Peltye va F.Majanda tomonidan 1817-yilda ajratilgan. U amyoba
dizenteriyasida, alveolyar pioreidada va boshqa amyoba kasalliklarida ishlatiladi.
Emetin qayt qildiradigan va balg‘am ko‘chiruvchi vositadir.](/data/documents/c49d4c8e-34dd-4933-848d-80060630b84f/page_32.png)



![36
singletlar bo ‘ lib, u H – 4' va H-5' ga tegishli. 6,91 m.u. dagi bitta protonli triplet J=5,1
NH guruhga tegishli. 7,21 m.u. da bitta protonli singlet H-6' ga tegishli.
Birikma Brutto formula Rf
t.suy, o
C
1
C
16 H
21 N
3 O
2 0,61 192-194;
194-195 [42]
2
0,66
3
0,7
4 0,73
5
0,77
6
0,84](/data/documents/c49d4c8e-34dd-4933-848d-80060630b84f/page_36.png)
![37
IV.TAJRIBAVIY QISM
Ajratish va tozalash uchun kerakli toza (absolyutlashtirilgan) erituvchilar olindi:
etanol, metanol, xloroform. Sintez qilib olingan moddalarning fizik – kimyoviy va
spektral kattaliklari tahlil qilindi. Asosan suyuqlanish temperaturasi, turli erituvchilar
sistemasida olingan yupqa qatlamli xromatogramma natijalari ya’ni R
f qiymatlari
aniqlandi. Etanol va metanolni absolyutlashtirish qoidaga binoan amalga oshirildi.
Olib borilayotgan sintez va sintez mahsulotlari yupqa qatlamli xromatogrammada
nazorat qilib turildi. Erituvchilar sistemasi sifatida xloroform – metanolni har xil
nisbatlarda olindi. Adsorbent sifatida silikogelning L5/40 markasini (13% li gips)
suvda tayyorlab shisha plastinkalarda maxsus qurilma yordamida yotqizib chiqildi.
Erituvchilar sistemasi sifatida quyidagilar olindi: 1sistema (xloroform-metanol 3:1), 2
sistema (xloroform-metanol 4:1).
Reaksiya mahsulotlarini xromatogrammada aniqlash uchun ochuvchi reagent
sifatida UB lampa, yodli kamera va Dragendorf eritmasidan foydalanildi. [79]
Ajratib olingan birikmalarining PMR spektrlari ham olindi.
1
H YaMR spektrlar 400 М Hz , м.д., J/ Hz da va erituvchilar sifatida
deytroxloroform, deytrometan, triftor sirka kislotasi ishlatildi. Ichki standart sifatida
geksametildisiloksan olindi. Natijalar muhokamasi qismida ularning PMR spektrlari
o‘rganildi. Bunda barcha tozalash, qayta kristallashlardan keyin qolgan reaksiya
mahsuloti induvidual bo’lgani uchun spektral tahlil uchun ishlatildi.
O‘simlik materialini tayyorlash. To liq pishgan goji mevalari (ʻ Lycium
depressum ) 2022-yil sentabr oyida Surxondaryo viloyatida joylashgan dala
hududidan yig‘ib olingan. O simlik botanik olima N.Nurillayeva tomonidan
ʻ
yig‘ilgan, quritilgan va sinov namunasi laboratoriyada saqlashga topshirilgan.
Olingan mevalar 48 soat davomida 40°C da termostatda quritish uchun qoldiriladi.
Olingan quruq material elektr blender yordamida maydalandi va keyingi tajriba
jarayonlari uchun 10 g miqdorda o‘lchab olindi.](/data/documents/c49d4c8e-34dd-4933-848d-80060630b84f/page_37.png)








1 LYCIUM DEPRESSUM MEVASINING ALKOLOID TARKIBINI O ‘RGANISH MUNDARIJA I . KIRISH ……………………………………………………………………. 3 II . А DABIYOTLAR SHARHI 2 .1. Alkaloidlar tasnifi ………………………………………………….. 5 2.2. Lycium turkum i tarkibidagi alkaloidlarining asosiy guruhlari.....…. 9 2.3. Lycium turkumining kimyoviy tarkibi ……….………………….... 1 4 2.4. Lycium turkumi optik faol alkaloidlari ………… ……………. ……. 25 2. 5 . Lycium turkumi tarkibidan ajratilgan alkaloidlarning biologik faolligi va farmakologik xususiyatlari …………… ………..... …... 30 III . NATIJALAR MUHOKAMASI …………. ……………………………. 35 IV . TAJRIBAVIY QISM …………………………………………………… 38 V. XULOSA ………………………………………………………………… 40 FOYDALANILGAN ADABIYOTLAR ………………………………... 41
2 I. KIRISH Ko‘plab dorivor o‘simliklar asosiy tarkibiy qismini alkaloidlar tashkil qiladi. Ular asos xarakteriga ega tarkibida azot saqlagan geterohalqali birikmalarning vakillaridir. Alkaloidlarga boy juda ko‘p o‘simlik oilalari o‘rganilgan. Lycium turkumi ham alkaloidlarga boy o‘simliklardan hisoblanadi. Mavzuning dolzarbligi va mohiyati. Hozirgi paytda tibbiyotda juda ko‘p alkaloidlar turli maqsadlarda ishlatilmoqda. Ayniqsa, dorivor vositalar sifatida. Ular asosan o‘simlik manbalaridan olingan yoki biror sintez asosida yaratilgan. Ammo, hamma vaqt insonlar uchun tabiiy, ekologik jihatdan toza va hech qanday zararli ta’sirlarga ega bo‘lmagan dorivor vositalarni izlash maqsadida tabiiy manbalarga murojaat etiladi. Bunday manbalar orasida floramiz biologik faol birikmalarga juda boydir. Bu esa kimyogarlar oldiga yangidan-yangi faol birikmalarni ochish va tinimsiz izlanishlarni amalga oshirish kabi muhim vazifani qo‘yadi. Tadqiqot obyekti sifatida o‘simliklar tanlangan hollarda bir necha bosqichli usullarda biologik material qayta ishlanadi. O‘simlik va birikmalar tabiatiga mos holda shart-sharoit larni o’rganish hamda mahsulotni toza holda ajratib olib spektral analiz va farmakologik tekshiruvlar uchun namunalar tayyorla nadi . Qattiq namuna ekstraksiyasi uchun ma’qbul usulni tanlash maqsadida jarayon 3 ta farqli sharoitlarda olib borildi. Tadqiqotning obyekti va predmeti. Tadqiqot obyekti sifatida Lycium depressum o‘simligi quritilgan mevalari olingan. Tadqiqot predmeti meva tarkibidan ajratib olinadigan asos xossalari alkaloidlar bo‘lib xizmat qiladi. Tadqiqotning ilmiy yangiligi. Ko‘plab adabiyotlar tahlili shuni ko‘rsatdiki Lycium turkumi vakillarining asosan 7 turi keng tarqalgan va oziq-ovqat mahsuloti hamda dorivor xususiyatga ega vosita sifatida keng foydalaniladi. Amaliy ahamiyati yuqori bo‘lgan ushbu turkum vakillari birmuncha o‘rganilgan bo‘lsa-da, geografik jihatdan tor doirada tarqalgan L.depressum turi nisbatan kam o‘rganilgan. Uning kimyoviy tarkibi bo‘yicha adabiyot ma’lumotlari yetarli emas. Bizning bu ishimizda Respublikamiz janubiy hududlarida tabiiy holda o‘sadigan Lycium depressum ning
3 alkaloid tarkibi o‘rganilgan. Ajratish jarayonida suvli fraksiyada 6 ta farqli Rf qiymatiga ega dog‘ lar aniqlandi. Shulardan bi ttas i ajratib olindi va xossalari o‘rganildi . Tadqiqotning ilmiy ahamiyati. Lycium depressum yetilgan mevalari tarkibidan alkaloidlarni ajratib olish maqsadida uch xil sharoitda qattiq namuna ekstraksiyasi amalaga oshirildi. Olingan spirtli ekstrakt qutbliligi jihatdan farqli erituvchilarda fraksiyalarga ajratildi. Suvli va etilasetatli fraksiyalar tarkibida n mahsulot ajratildi va tozalandi . Bu esa olib borilgan sintezning ham nazari y , ham amaliy jihatdan muhimligini bildiradi. Ish Organik sintez va bioorganik kimyo kafedrasi ilmiy laboratoriyasida bajarilgan. Bitiruv malakaviy ishning tuzilishi va hajmi . Mazkur bitiruv malakaviy ishi kirish, adabyoitlar sharhi, tajribaviy qismdan iborat, uch bobda rasmiylashtirilgan bo‘lib, 5 ta jadval, 69 ta nomdagi foydalanilgan adabiyotlar ro‘yxatida iborat 46 betda rasmiylashtirilgan.
4 II. ADABIYOTLAR SHARHI 2.1. Alkaloidlar tasnif i Hozirgi vaqtda 10000 ga yaqin alkaloidlar turi bo‘lib, ulardan 4000 tasining tuzilishi isbotlangan [1-3]. Bunday ko‘p miqdor alkaloidlarni turlicha sinflashga sabab bo‘lmoqda. Alkaloidlarni sinflashning bir qancha prinsiplari bo‘lib, ularning ayrimlari quyida keltirilgan. Alkaloidlarni farmakologik xossalariga ko‘ra klassifikatsiyalashda ularning organizmga ta’siri asos qilib olinadi: - narkotik alkaloidlar; - mahalliy og‘riqsizlantiruvchi alkaloidlar; - spazmalitik alkaloidlar; - kurarega o‘xshash (farmakologik ta’siri) ta’sirga ega alkaloidlar. Botanik klassifikatsiyalash asosida esa o‘simlik oilalari asos qilib olinib, ulardan ajratib olingan alkaloidlar birgalikda guruhlanadi: - tamakidoshlar alkaloidlari; - lolaguldoshlar alkaloidlari; - sporinlar alkaloidlari. Bu klassifikatsiyalar alkaloidlarning kimyoviy tuzilishini e’tiborga olmaydi. Angliyalik olim Xegnauer biogenetik klassifikatsiyani taklif qildi. Bu klassifikatsiyada alkaloidlarning biosintez yo‘liga e’tibor qaratiladi, ya’ni alkaloidlar hosil bo‘lishida ishtirok etayotgan aminokislotalar asosiy hisoblanadi. Shunga ko‘ra quyidagi alkaoidlar guruhlari ajratiladi: - triptofan alkaloidlari; - fenilalanin alkaloidlari. 1910-yilda E.Vintershteyn va T.Trir alkaloidlar to‘g‘risidagi zamonaviy tushunchalarni izohlab, haqiqiy alkaloid bo‘lishi uchun quyidagi to‘rt shart bajarilishi kerak deb e’tirof etadilar. 1. Azot atomi geterosiklik halqa tarkibida bo‘lishi kerak; 2. Birikma murakkab molekulyar strukturaga ega bo‘lishi kerak;
5 3. Ular albatta farmakologik faol bo‘lishi kerak; 4. O‘simlik tarkibida bo‘lishi kerak . Lekin barcha alakaloidlar ham bu talablarga javob bera olmaydi. Kolxitsin, piperin kabi alkaloidlar asos xarakteriga ega emas. Kolxitsin meskalin va feniletilamin singarilar geterosiklik birikma hisoblanmaydi [4]. Professor V.S.Sokolov [5] alkaloidlar uchraydigan o‘simlik oilalarini hisobga olib, alkaloid saqlagan o‘simliklarni 3 guruhga ajratadi: 1 guruh oilalar – 20% dan kam bo‘lmagan alkaloid saqlagan o‘simliklar oilalari. Bu oilalarni Sokolov alkaloidlarga boy oilalar deb atadi. 2 guruh oilalar – 10% dan 20 % gacha alkaloid saqlagan o‘simliklar oilalari. Bu oilalar – o‘rtacha alkaloidli hisoblanadi. 3 guruh oilalar – 1% dan 10 % gacha alkaloid saqlagan o‘simliklar oilalari. Bunday oilalar –kam alkaloidli hisoblanadi. Hozirgi vaqtada molekulada azot atomining joylashishiga qarab alkaloidlar quyidagi guruhlarga ajratiladi: 1. Haqiqiy alkaloidlar – azot atomi tutgan geterosiklik birikmalar va aminokislotalardan tashkil topgan birikmalar (giosiamin, kofein, platifillin). 2. Protoalkaloidlar – yon zanjirida azot saqlagan alifatik birikmalar va aminokislotalardan tashkil topgan birikmalar (efedrin, kapsaitsin). 3. Psevdoalkaloidlar – terpen va steroid tabiatli azot saqlagan birikmalar (sоlаsоdin). Ko‘pincha farmakognoziyada akad.A.P.Orexov taklif qilgan kimyoviy klassifikatsiyadan foydalaniladi. Bu klassifikatsiya asosida asosan azot saqlagan geterosiklik tuzilishli alkaloidning kimyoviy tuzilishi yotadi.
